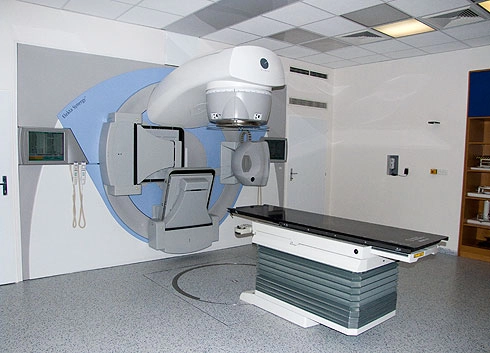
Jak probíhá ozařování
Nádorů hlavy a krku v posledním desetiletí na celém světě dramaticky přibývá. Týká se to zejména žen. Výskyt nových případů nádorů v oblasti hlavy a krku se celosvětově odhaduje na 363 000 případů ročně, přičemž počet úmrtí činí 200 000 za rok. V Evropě se za rok vyskytne kolem 140 000 případů. Nádory hlavy a krku představují v zemích EU čtvrtý nejčastější nádor u mužů. Výskyt je charakterizován stoupajícím množstvím od severu směrem ke Středozemnímu moři. V současnosti se nádory hlavy a krku léčí pomocí chirurgie, radioterapie nebo kombinací obojího. Z prováděných výzkumů vyplývá, že tato léčba může být nedostačující, a proto se v některých případech přistupuje k takzvané optimální léčbě. To znamená, že se k léčbě využívá kombinace chirurgie, ozařování nádorů a chemoterapie a někdy také biologická léčba.
Radioterapie spolu s chirurgickou léčbou patří mezi hlavní lokoregionálně působící metody onkologické léčby. Žádná z těchto metod však nemůže postihnout vzdálený nádorový rozsev, a proto jsou tyto metody základem léčby především u časných lokalizovaných stadií onemocnění. V dnešní radioterapii se využívá moderních ozařovačů disponujících možnostmi tvarování polí, technikami IMRT či IGRT, nebo nových plánovacích jednotek využívajících metod inverzního plánování. Tento technický pokrok vede k naplnění vize konformní radioterapie (maximální přizpůsobení tvaru ozařovaného objemu nepravidelnému tvaru nádoru). Účinek záření na tkáně a orgány není dán jen celkovou aplikovanou dávkou záření, ale také jejím časovým rozložením, takzvanou frakcionací. Nové frakcionační režimy rovněž zvyšují efekt léčby. Léčebnou účinnost radioterapie lze posílit i její vhodnou kombinací s ostatními metodami protinádorové léčby.
Potíže po ozařování hlavy a krku, je hlavní myšlenka, která vedla k vytvoření tohoto článku. Můžete se dozvědět i širší souvislosti, zde je výběr nejlepších momentů souvisejících s tématem následky po ozařování
Také se můžete podívat na článek Ozařování a dozvědět se další související informace.
Konformní techniky radioterapie
Konformní techniky ozáření (conform = přizpůsobit) mají za cíl přizpůsobit tvar ozařovaného objemu nepravidelnému tvaru nádoru. Důsledkem je potom stupňování dávky bez rizika poškození zdravých tkání v okolí. Zvýšení dávky záření v ložisku jednoznačně zvyšuje lokální kontrolu nádoru. Zvýšená lokální kontrola potom prodlužuje celkovou dobu přežití pacienta. Při dříve používaných konvenčních technikách měl ozařovaný objem pravidelný tvar, například válce nebo kvádru. Tento objem zahrnoval nepravidelně tvarovaný tumor a okolní zdravé tkáně v neoptimální míře, čímž docházelo ke vzniku nežádoucích účinků, které vyplývaly z poškození těchto tkání. Při konformní radioterapii je ozařovaný objem upravován prostorově ve třech rovinách (3D), čímž se více přizpůsobí tvaru nádoru. Výsledkem je redukce celkového objemu ozařovaných tkání. Tím se sníží míra rizika nežádoucích účinků a možnost aplikace vyšší dávky do samotné nádorové masy a zvýšení účinnosti radioterapie. Tyto techniky tedy umožňují přesnějším plánováním a provedením ozáření zredukovat velikost bezpečnostního lemu okolo vlastního nádorového ložiska a tím ve srovnání s technikami konvenčními snížit velikost ozářeného objemu o 20–30 %. Ke geometrickému tvarování svazků záření byly v dřívějších letech používány takzvané vykrývací bloky připravené na míru. Tyto bloky se připravovaly ze speciálního kovu pro každého pacienta individuálně. V dnešní době mají moderní přístroje k dispozici „vícelamelový kolimátor“, tudíž mohou pracovat s různě tvarovanými poli i bez použití těchto bloků. Konformní techniky radioterapie jsou v dnešní době nutným standardem v radioterapii nádorů hlavy a krku. Konvenční techniky radioterapie je možné použít pouze za účelem paliativním či k symptomatickému ovlivnění potíží pacientů.
Radioterapie s modulovanou intenzitou IMRT
Dalším stupněm technického pokroku v radioterapii se staly techniky IMRT (intensity-modulated radiation therapy). Stejně jako výše popisované konformní techniky používají i techniky IMRT geometricky tvarované svazky záření, ale tyto svazky nemají v celém svém objemu stejnou intenzitu. Plánovací systém rozdělí svazek záření na jednotlivé části a každé z nich přiřadí určitou intenzitu tak, aby co nejlépe vyhověl zadaným kritériím. Vhodnou kombinací svazků a změnou intenzity jejich částí systém docílí výrazně lepší prostorové distribuce dávky než jiné metody. Změna intenzity a tvaru jednotlivých svazků se děje na základě pohybu lamel kolimátoru. Plánování radioterapie vychází z dat získaných při plánovacím CT vyšetření. Toto snímkování je nezbytné provádět v poloze, v níž bude pacient ozařován, a s použitím všech zhotovených fixačních pomůcek. Dalším krokem při plánování je zakreslení kontur cílových objemů a rizikových struktur. Pomocí zobrazovacích diagnostických metod (CT, MRI, eventuálně PET) je přesně detekováno nádorové ložisko a okolní rizikové orgány. Trojrozměrná rekonstrukce obrazu je převedena do plánovacího systému, kde jsou zakresleny jednotlivé cílové objemy. Po zakreslení se specifikují požadované dávky do cílových objemů a dávkové limity pro zdravé tkáně a orgány. Dále se plánovacímu systému určí „váha“, s jakou je povinen dodržet jednotlivé limity. Zpravidla má nejvyšší váhu dodržení dávky v cílovém objemu, nicméně i limity ozáření některých kritických orgánů mohou mít váhu velmi vysokou. Následně již plánovací systém vypočítá rozložení dávky. Výsledkem je plán, který s maximální dosažitelnou přesností dodržuje předepsané rozložení dávky v cílovém objemu, přičemž dávky v kritických orgánech jsou pod stanovenými limity.
Jestli se zajímáte i o další informace, tak zpracované téma následky po ozařování krku je výběr toho nedůležitějšího, co jsme na toto téma napsali. Mnohdy nám k tomu pomohly i zkušenosti a rady ostatních uživatelů.
Za zmínku stojí také článek Suché vlasy.
Obrazem řízená radioterapie IGRT
Pro kontrolu polohy pacienta na ozařovacím stole je dnes již standardně používán portálový verifikační systém. Jedná se o přídavné elektronické zařízení k lineárnímu urychlovači, které dovoluje zobrazit umístění ozařovacího pole na pacientovi při reálných ozařovacích podmínkách, a tím zkontrolovat pozici izocentra. Speciální detektor umožňuje dvojdimenzionálně zobrazit anatomické (kostní) struktury pacienta z pohledu svazku záření a srovnat je se stejným pohledem vygenerovaným automaticky plánovacím systémem. Nadlimitní neshody je možné na místě korigovat. Nejmodernější lineární urychlovače jsou dnes rovněž vybavovány systémem umožňujícím přesnou kontrolu polohy pacienta na ozařovacím stole ve všech třech rovinách. Tento systém je tvořen počítačovým tomografem (CT) zabudovaným přímo do lineárního urychlovače. Je schopen přesně prostorově zobrazit cílový objem v okamžiku ozařování. Na rozdíl od klasických CT přístrojů je tento systém schopen nasbírat všechna potřebná data během jediného otočení ramene kolem pacienta. Po ukončení rotace hlavice je získán trojrozměrný objemový obraz pacienta, který odpovídá skutečnosti v okamžiku ozařování. Informace o aktuálním rozložení tkání v okolí cílového objemu je možné porovnat s původními informacemi, na jejichž základě byl vytvořen ozařovací plán. Zjištěnou odchylku je možné napravit dvěma způsoby:
- ON LINE – systém poskytne údaje potřebné ke korekci nastavení pacienta pomocí pohybů ozařovacího stolu. Jakmile jsou potřebné korekce stolu provedeny, může ozáření se zajištěním maximálně přesného cílení a nastavení proběhnout.
- OFF LINE – změny v pacientově anatomii jsou přeneseny do plánovacího systému a následně je vytvořen nový plán přizpůsobený nové poloze pacienta. Metoda IGRT dává možnost přesně identifikovat tumor a kritické struktury a aplikovat dávku záření s maximální přesností. Ve spojení s náročnými ozařovacími technikami může metoda obrazem řízené radioterapie zlepšit výsledky léčby pacientů v klinické praxi.
Rozložení dávky v čase (frakcionace)
Účinek záření na tkáně a orgány není dán jen celkovou aplikovanou dávkou, ale také jejím časovým rozložením, takzvanou frakcionací. Právě alterované frakcionační režimy jsou s úspěchem využívány u nádorů hlavy a krku. Rozlišují se tyto základní typy frakcionace: standardní frakcionace, kdy se aplikuje dávka 1,8–2,0 Gy jednou denně 5krát týdně; hypofrakcionace, při které se ozařuje vyšší jednotlivou dávkou méně než 5x za týden; hyperfrakcionace, kdy se aplikuje menší jednotlivá dávka ve více než pěti frakcích za týden, to znamená, že se ozařuje několikrát denně. Aby byla dávka biologicky ekvivalentní, je při tomto režimu nutné aplikovat dávku celkově vyšší než při standardní frakcionaci. Celkový čas léčby se výrazně nemění; akcelerovaná frakcionace znamená ozáření v celkově kratším čase, přičemž celková dávka ani počet frakcí nejsou významně změněny. Akcelerovaná hyperfrakcionace spojuje znaky obou uvedených typů frakcionace dohromady. Typické konvenční radioterapeutické protokoly doporučují používat standardní frakcionaci, což znamená aplikovat celkovou dávku 60–70 Gy frakcionovaně po 1,8–2,0 Gy 1x denně od pondělí do pátku v průběhu 6–7 týdnů. Několik studií však naznačilo, že lokální kontrola nádorů hlavy a krku může být zlepšena zvýšením celkové dávky a zkrácením celkové doby ozařování. Základní výhodou hyperfrakcionačních schémat je, že použití více frakcí menších dávek umožňuje docílit vyšší celkové dávky, aniž by se překročily toleranční dávky pozdně reagujících tkaní, jejichž poškození může výrazně zhoršit kvalitu života pacientů po úspěšně dokončené terapii (mícha, cévy, podkožní vazivo). Takové ozáření je biologicky účinnější na nádor, ale samozřejmě způsobuje výraznější vedlejší účinky u časně reagujících tkání. Proto je nedílnou součástí léčby pečlivé ošetřování akutních reakcí zejména na sliznicích a kůži. Čím více je frakcí, tím větší je šance, že nádorové buňky přejdou při další frakci z radiorezistentní fáze buněčného cyklu do fáze senzitivnější. Vzhledem k tomu, že efekt hyperfrakcionace je méně závislý na kyslíkovém efektu, je tato léčba účinnější i na hypoxické buňky. Při akcelerované radioterapii vlivem kratší celkové doby terapie klesá možnost regenerace nádorových buněk mezi jednotlivými frakcemi a zároveň stoupá pravděpodobnost kontroly nádoru. Jelikož celkový čas nemá vliv na poškození pozdně reagujících tkání, výsledným efektem by měla být terapie a zisk.
Pro ty z vás, kteří chtějí více informací na jednom místě, jsme vybrali podstatné inforamce a seřadili jsme je do jedné ucelené stránky, kterou najdete zde: vše podstatné týkající se tématu ozařování hlavy, a přidali jsme i příběhy ostatních čtenářů.
Článek Vše o vlasech by také mohl pomoci rozšířit povědomí o nové poznatky.
Simultánní integrovaný boost (SIB)
V posledních letech byla do praxe zavedena technika takzvaného simultánního integrovaného boostu (SIB). Principem této metody je možnost navýšit jednotlivé, případně i celkové dávky v části ozařovaného objemu, kde je z hlediska nádorového onemocnění největší riziko (makroskopický tumor, postižené lymfatické uzliny či lůžko nádoru). Zbylá část cílového objemu se ozařuje standardní dávkou. Použití této techniky vyžaduje moderní technologické zázemí s výkonným plánovacím systémem, lineárním urychlovačem umožňujícím techniku IMRT a korekci polohy pacienta přímo na ozařovacím stole (IGRT). SIB má několik výhod – v průběhu léčby pacienta se lze vyhnout komplikovanému postupnému zmenšování cílového objemu, které je standardem u mnoha konvenčních i konformních technik ozáření. Ve srovnání s konvenčními technikami je při použití SIB nižší celková integrální dávka a vyšší konformita distribuce dávky v cílovém objemu. Z hlediska radiobiologie je nespornou výhodou zkrácení celkové doby ozařování.
Adaptivní radioterapie
Plánování radioterapie je založeno na obrazových informacích získaných při zahájení léčby. Na základě těchto dat je vytvořen ozařovací plán, který je následně používán po celou dobu ozařování pacienta. V průběhu léčby však díky zmenšování nádoru, ztrátě hmotnosti pacienta a otoku měkkých tkání může dojít ke změnám anatomie ozařované oblasti. Tyto změny mohou být významné zejména při použití moderních technik záření, které jsou charakterizovány prudkým spádem dávky mezi masou tumoru a zdravými tkáněmi v okolí. Anatomické rozdíly mohou způsobit přezáření citlivých struktur či nedozáření tumoru a postižených uzlin. Adaptivní radioterapie je založena na provedení nového plánování v průběhu ozařovacího cyklu tak, aby se léčba lépe přizpůsobila novým anatomickým poměrům. Zatím však není jasné, kdy a jak často tuto úpravu dělat. Rovněž je nutné počítat s technickými problémy a nedostatkem času, navíc potřebným k novému plánování. Než dojde k rozšíření těchto metod adaptivní radioterapie, budou nutné nové technologie automatické registrace obrazu, automatické kontumace cílových objemů a plánovací stanice s vyšším výkonem. V současné době se přeplánování neprovádí rutinně, pouze při evidentních anatomických změnách v průběhu léčby.
Potíže po ozařování hlavy a krku, je hlavní myšlenka, která vedla k vytvoření tohoto článku. Můžete se dozvědět i širší souvislosti, zde je výběr nejlepších momentů souvisejících s tématem následky ozařování
Také se můžete podívat na článek Jak nagelovat vlasy a dozvědět se další související informace.
Brachyterapie
Při brachyradioterapii je radioaktivní zdroj záření umístěn přímo v oblasti nádoru, kde se tak koncentruje vysoká dávka záření (nitrodutinové zavádění zářičů nebo tkáňové punktury). Spád dávky s rostoucí vzdáleností od zdroje je velmi rychlý a zdravé tkáně obklopující nádorové ložisko jsou zatíženy podstatně nižší dávkou než nádor samotný. O aplikaci brachyradioterapie je nutno uvažovat všude tam, kde je ložisko snadno přístupné a má relativně malý objem. Lze ji použít buď jako jediný prostředek léčby k dosažení radikální dávky, nebo v kombinaci s chirurgickým výkonem. Implantace radionuklidu může být provedena i pooperačně. Je možno použít tuto techniku u nádorů jazyka, rtů (kurativní u stadia T1 a T2), dále většinou paliativní u nádorů tonzily, měkkého patra, u metastatického postižení krčních uzlin. Intrakavitární brachyterapii jako boost techniku je možné použít u nádorů nazofaryngu. Zpočátku se v brachyradioterapii používaly pouze radiové tuby a jehly. Radium však bylo nahrazeno jinými radionuklidy a k zavádění se využívá dálkově ovládané zařízení – afterloading. Pro intersticiální implantace je používáno nejčastěji 192Ir – iridium. Pro některé lokalizace nádorového onemocnění, kde by bylo obtížné odstranit implantované zdroje záření a kde lze s výhodou využít vysoký dávkový příkon, se aplikují krátkodobé zdroje záření jako 125I nebo 198Au (permanentní implantace radioaktivních zrn).
Léčba může probíhat buď formou ambulantní, nebo při hospitalizaci v onkologickém centru. Pro ambulantně léčené pacienty je pro případ nenadálých obtíží nepřetržitě k dispozici lékař, zajišťující službu pro onkologické centrum.
Následky po ozařování
Tolerance radioterapie je individuální a nežádoucí účinky se mohou projevit v různé míře. Pokud budete mít potíže spojené s ozářením, doporučí vám lékař vhodná opatření a předepíše potřebné léky. U mnohých nemocných je však tolerance léčby natolik dobrá, že nejsou třeba žádná omezení, a pokud to organizační podmínky dovolí, není nezbytně nutná ani pracovní neschopnost. Jako celková reakce organismu na ozáření by se mohla vyskytnout únava a ospalost, nechutenství, výjimečně nevolnost.
Při užití vysokoenergetického zdroje záření se již méně často objevuje poradiační reakce na kůži, která se může projevit zarudnutím pokožky. Je důležité pokožku nedráždit a vzdušnit a nosit pokud možno bavlněné prádlo. Při ozáření některých lokalit, například v oblasti prsu či hlavy a krku, však může být kožní reakce výraznější. Může dojít k olupování, vzácněji i k mokvání pokožky.
Časný erytém na kůži vzniká u citlivých jedinců již 2. až 3. den po započetí ozařování. Pozdní erytém se objevuje mezi 2. až 4. týdnem, je výrazně tmavší a přechází do pigmentace a suché deskvamace (kůže je sušší, drobně se olupuje) nebo přechází do reakce 2. stupně — vlhké deskvamace.
Za zmínku stojí také článek Péče o barvené vlasy.
Ošetřování při akutní fázi
Je důležité chránit kůži před mechanickými vlivy a dalším drážděním – náplasti, mýdla, parfémy, nenosit neprodyšný oděv. Kůži promazávejte nejdříve 2 hodiny po ozáření. Ozařovaná místa se nemají umývat mýdlem. K omývání jsou vhodné například termální vody ke zklidnění pokožky. K promazávání se doporučují mastné masti typu Calcium panthotenicum, Panthenol gel; léčebná kosmetika je k dostání v lékárnách. Je možné přikládat chladicí gelové termopolštářky. Není vhodné používat rostlinné výtažky, protože často alergizují. Možno aplikovat i speciální krytí k vlhkému hojení ran po domluvě s dermatologem, například Mepilex, Sanavel, Mepitel, Inadine. Ošetřování poradiační reakce vždy konzultujte se svým lékařem. Záření může mít vliv na krvetvorbu, může dojít ke snížení počtu krvinek, zejména bílých. Díky těmto změnám v krevním obrazu můžete mít větší náchylnost k infekčním nemocem, proto je vhodné omezit návštěvy velkých kolektivů a je také nutné vyhýbat se lidem se známkami infekčních onemocnění (rýma, kašel a podobně). Během léčby se mohou objevit i poruchy spánku, které mohou mít vliv na další zhoršení únavy. Charakter místních příznaků závisí na oblasti, která je ozařována. Mohou se vyskytnout v různé intenzitě.
Akutně se může během ozařování objevit kožní reakce podobná přehnanému opalování na sluníčku. Kůže zčervená, mírně zduří, je citlivější na dotek, svědí. Může se objevit i suché olupování nebo až mokvání pokožky (především v kožních řasách). Ke konci se objevuje ztmavnutí kůže. Ve vlasatých a ochlupených částech lidského těla dochází na ozařovaných polích k vypadávání vlasů, chlupů a vousů.
V dutině ústní se v průběhu léčby objevuje zpočátku přechodně větší slinění. Poté se dostavuje suchost v ústech, sliny jsou lepkavé, chuťové vjemy se ztrácejí nebo se mění v různé pachutě. Někdy dochází k úplné zástavě tvorby slin, i těch vazkých. Zhoršuje se polykání zejména objemných a tvrdých soust. Po ukončení ozařování (až do 2–3 let) se mohou objevit pozdní nežádoucí účinky léčby zářením, například kožní změny (zarudnutí, pigmentace, suchá a méně elastická kůže), tužší podkoží, podkožní otok v oblasti krku a pod bradou, suchost v dutině ústní, snížení funkce štítné žlázy. Ztuhnutí čelistního kloubu (trismu) lze předcházet cvičením otvírání úst.
Nežádoucí účinky ozařování mozku
Ozařování (radioterapie) patří mezi základní léčebné metody, které se používají k léčbě nádoru mozku (nádor na mozku). Ozařování může být použito jako metoda doplňková po operačním výkonu nebo jako metoda hlavní, kdy operační výkon není pro lokalizaci, pokročilost nebo typ nádoru vhodný. Ozařování je metoda, která poškozuje i zdravé buňky, ty jsou však více odolné než buňky nádorové. Rozlišují se dvě základní metody radioterapie, a to vnější, kdy zdroj záření (ozařovač) je mimo tělo pacienta, a vnitřní, kdy se radioaktivní materiál dává při operaci do lebky do nádoru nebo jeho lůžka. V České republice se vnitřní ozařování (brachyradioterapie) nepoužívá a rovněž ve světě je dominantní ozařování vnější (teleradioterapie).
Vnější ozařování (teleradioterapie) – záření vychází z vnějšku z ozařovacího přístroje do mozku. Lékařem-radioterapeutem je předem jasně definováno, jak velké bude ozařovací pole (ozářená část mozku), jak velká bude dávka záření a v kolika sezeních bude ozařování probíhat. Vše je stanoveno s ohledem na velikost nádoru, jeho typ, lokalizaci a celkový stav pacienta. Délka ozařování se zpravidla pohybuje mezi třemi až šesti týdny. Během této doby pacient při standardním ozařování dochází do ozařovny pětkrát za týden. Doba jedné denní dávky (takzvaná frakce) trvá přibližně 3–6 minut. Aby bylo ozařovací pole vždy stejné, tedy aby se ozařovala vždy stejná část mozku, bývá hlava upevněna v umělohmotné masce.
Stereotaktická radiochirurgie – forma vnějšího ozařování určená k intenzivní léčbě malých nádorů (do 3 cm). Pomocí speciálního zaměřovacího a fixačního zařízení může být do malé postižené oblasti podána poměrně vysoká dávka záření s minimálním rizikem poškození okolních zdravých tkání.
Vedlejší účinky ozařování – obecně je můžeme rozdělit na časné a pozdní. Mezi časné patří zvýšená únava, slabost, bolesti hlavy, nechutenství a někdy i zvracení. Po ukončení ozařování tyto potíže mizí. Častým vedlejším účinkem je i vypadávání vlasů, které se objevuje cca po dvou až třech týdnech ozařování a bývá omezené na ozařované pole. Vypadávání vlasů bývá většinou dočasné, při vyšších dávkách záření však může být i trvalé. Mezi pozdní vedlejší účinky se řadí poruchy paměti a koncentrace, ty vznikají za 1–3 roky po ozařování a dlouhodobě přetrvávají.
Příznaky metastáz do mozku a následně vyšetření se v zásadě neliší od primárních nádorů mozku. Léčebné metody jsou rovněž v podstatě stejné. O tom, jaké metody budou k léčbě použity, v jakém pořadí a s jakou intenzitou, rozhoduje četnost metastáz, jejich velikost, lokalizace, rozsah a histologický typ základního onemocnění a především celkový stav pacienta.
Nádorové onemocnění mozku představuje pro pacienta i jeho okolí závažný problém. Nelze vždy předvídat, do jaké míry bude léčba úspěšná a zda vrátí nemocného do normálního života.
Prognóza a přežití pacientů s nádory mozku závisí na mnoha okolnostech. Jedním z nejzásadnějších faktorů je histologický typ nádoru, možnost jeho radikálního odstranění operační cestou nebo zářením, citlivost k chemoterapii. Jsou nádory, které jsou dnešními metodami léčitelné a vyléčitelné, jako například meningeomy, adenomy hypofýzy, germinativní nádory a jiné. Na druhou stranu jsou zde skupiny nádorů mozku, u nichž je i přes sebevětší snahu a pokroky v onkologii pravděpodobnost vyléčení malá (například vysoce agresivní gliomy). Léčbou však lze aspoň prodloužit život nebo zmírnit příznaky onemocnění. O konkrétních možnostech léčby, jejích výsledcích, možných nežádoucích účincích a prognóze je nutno se poradit s lékařem.
Článek Jemné vlasy by také mohl pomoci rozšířit povědomí o nové poznatky.
Vedlejší účinky ozařování krku
Samotná terapie zatíží už i tak oslabený organismus. Jako vedlejší účinek radioterapie pacienti často udávají únavu, nechutenství, hubnutí a obecně špatný stav.
Protože ozařování proniká pokožkou, vedlejší účinky terapie jsou zde nejviditelnější. Typickým příznakem na zasaženém místě je vysušení, svědění, ale i ztráta ochlupení a vlasů. Kvůli zmírnění kožních problémů se v této době nedoporučuje používání mýdel s umělými přísadami, parfémů a jiných kosmetických přípravků. K mytí jsou nejlepší neutrální přípravky z přírodních složek, například organická mýdla. Na zmírnění podráždění a pálení mohou pomoci obklady se studenou vodou a chlazení pokožky. Je velmi důležité vyhýbat se po chemoterapii slunečnímu záření. Ani po uplynutí jednoho roku se nesmí citlivá pokožka opalovat. Vypadávání vlasů je pouze přechodné, ale opětovný růst začne pomalu.
Pokud se paprsky ozařování dotýkají i sliznice, která obklopuje duté orgány, může v těchto místech vzniknout vyschnutí. Mezi časté vedlejší účinky ozařování hlavy nebo krku patří poruchy tvorby slin a také (dočasná) ztráta chuti a čichu. Typickým příznakem jsou i těžkosti s polykáním, což může dohromady s nechutenstvím vést k výrazné ztrátě hmotnosti. Proto v těchto případech lékař předpisuje léky, které podporují chuť k jídlu, a je potřebné zvýšit i příjem vitamínů a živin. Ozařování zvyšuje riziko dehydratace, a proto se doporučuje zvýšený příjem tekutin. Vedlejším účinkem radioterapie je také zánět sliznice, který se týká jícnu, ústní dutiny, žaludku a střev.
Dehydratace se může objevit nejenom při ozařování hlavy a krku, ale i po radioterapii, která se týká trávicího systému. Příčinou je průjem, který je v každém případě potřeba léčit. Řešením může být užívání probiotik a ještě lépe synbiotik, která obsahují probiotické bakterie i prebiotika. Italští vědci zjistili, že díky podávání mléčných bakterií se průjem jako následek ozařování objevuje méně často. Dobrým řešením je i zvýšený příjem vlákniny rozpustné ve vodě (pektin, inulin, betaglukan), které se nacházejí zejména v banánech, jablkách, artyčoku, hruškách, červené řepě, ovsu a dýni na pečení. V případě průjmu je potřeba vyhýbat se mléčným výrobkům a kofeinu.
Vypadávání vlasů po ozařování
Vypadávání vlasů je častým vedlejším účinkem u nádorů hlavy. Objevuje se po dvou až třech týdnech ozařování a bývá omezené na ozařovací pole.
Také se můžete podívat na článek Domácí masky pro extrémně poškozené vlasy a dozvědět se další související informace.
Co je zakázáno při ozařování
Podávání vysokých dávek antioxidantů může vést ke snížení pozitivních účinků radioterapie. Při ozařování v oblasti krku je zakázáno kouření, pacient nesmí jíst kořeněná či tuhá jídla, nesmí konzumovat alkohol. Zcela nevhodné je úplně měnit jídelníček, například vynechat maso, držet hladovku.
Autor: © Mgr. Světluše Vinšová
Foto: © Jan Procházka